
2021-2022 英语周报 高一 课标 16 hze答案

18.参考答案(1)>(1分)>(1分)(2)+110k/mol(2分)(3)①C2H4(2分)生成C2H4的反应为吸热反应,温度升高平衡正向移动C2H4的物质的量分数增大(2分)②ab(2分)③分(2分说明分析I.(1)该反应正反应为吸热反应活化能E3正>E道;温度升高,平衡向正反应方向移动,k正增大的倍数大于k逆增大的倍数Ⅱ.(2)根据盖斯定律,主反应i2副反应ⅱ可得副反应i:C2H5OC2H5(g)催化剂2C2H4(g)+H2O(g),则△H3=2△H1-△H2=(+45.5k/mo)(-19.0 kJ/mol)-+110 kJ/mol.(3)①根据主反应i和副反应ⅲ可知,生成乙烯的反应均为吸热反应,升高温度,平衡向正反应方向移动,乙烯的物质的量分数增大所以图中Y代表的是②a乙烯浓度不再变化,说明正、逆反应速率相等反应达到了平衡b该反应为气体分子数增大的反应,容器内压强不随时间变化,说明反应达到了平衡;c反应过程中气体总质量始终不变,总体积不变,混合气体的密度始终不变,所以混合气体的密度不随时间变化,不能说明反应达到了平衡;d.△H不随反应的进行而变化,故△H不变化,不能说明反应达到了平衡③平衡时设乙烯为xmo,乙醚为ymol,380℃时,由图像可知x=4y,由于乙醇完全消耗,根据元素守恒,n(C2H5OH)=n(C2H4)+2n(C2H5OC2H5),则x+解得4y,再根据氢元素守恒,n(H2O)10-4(C2H4)·c(H2O×4)mol3 mol Kc(C2 Hs OC2 H5)生m0l÷2L)2×(3mol÷2L)2m2nol÷2L
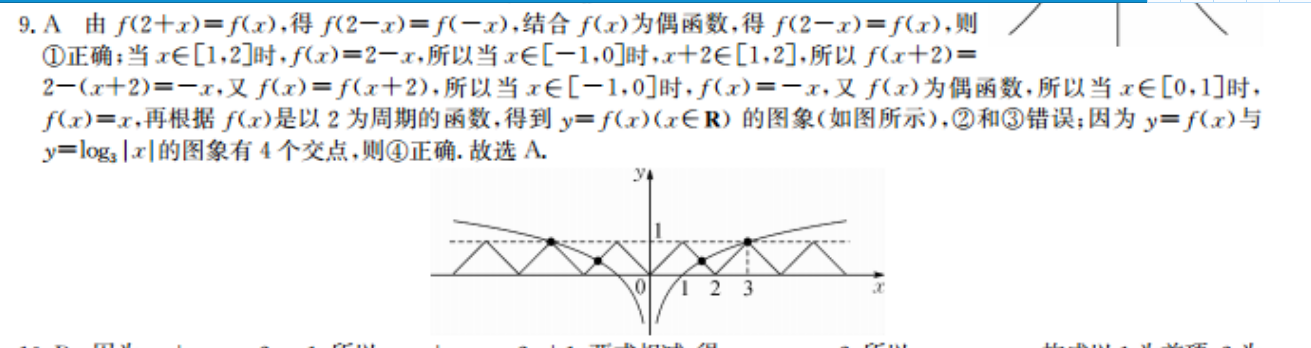
9.A由f(2+x)=f(x),得f(2-x)=f(-x),结合f(x)为偶函数,得f(2-x)=f(x),则①正确;当x∈[1,2]时,f(x)=2-x,所以当x∈[-1,0时,x+2∈[1,2],所以f(x+2)=2-(x+2)=-x,又f(x)=f(x+2),所以当x∈[-1,0]时,f(x)=-x,又f(x)为偶函数,所以当x∈[0,1]时,f(x)=x,再根据f(x)是以2为周期的函数,得到y=f(x)(x∈R)的图象(如图所示),②和③错误;因为y=f(x)与y=log|xl的图象有4个交点,则④正确.故选A

以上就是2021-2022 英语周报 高一 课标 16 hze答案,更多英语周报答案请关注本网站。
本文地址: http://www.ncneedu.cn/post/8952.html
文章来源:admin
版权声明:除非特别标注,否则均为本站原创文章,转载时请以链接形式注明文章出处。
- 04-05 1 英语周报八年级新目标答案第29期
- 04-05 2 英语周报八年级新目标scc答案5
- 04-05 3 英语周报答案七年级上册2022-2023
- 04-05 4 英语周报答案2022~2023
- 04-05 5 英语周报答案八年级下册2023
- 04-05 6 英语周报答案九年级人教版2023
- 02-24 7 时代英语报2022-2023 test7答案
- 02-24 8 双语报答案20222023高三
- 02-24 9 双语报浙江W版中考专版第35期答案
- 02-24 10 双语报英语答案高三课标24期
- 英语周报八年级新目标答案第29期
2023-04-05admin
- 英语周报八年级新目标scc答案5
2023-04-05admin
- 英语周报答案七年级上册2022-2023
2023-04-05admin
- 英语周报答案2022~2023
2023-04-05admin
- 英语周报答案八年级下册2023
2023-04-05admin
- 英语周报答案九年级人教版2023
2023-04-05admin
- 时代英语报2022-2023 test7答案
2023-02-24admin
- 双语报答案20222023高三
2023-02-24admin
- 双语报浙江W版中考专版第35期答案
2023-02-24admin
- 双语报英语答案高三课标24期
2023-02-24admin
