
英语周报高一3期答案2023
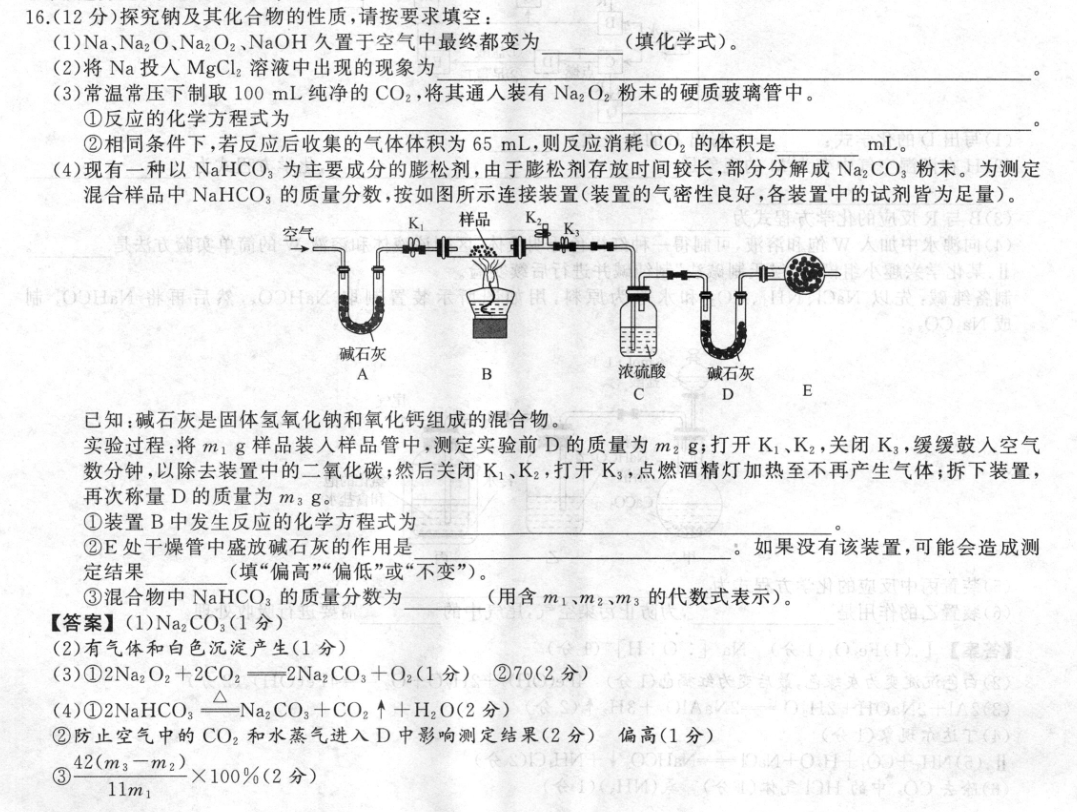

16.(12分)探究钠及其化合物的性质,请按要求填空:(1)Na、Na2O、Na2O2、NaOH久置于空气中最终都变为(填化学式)。(2)将Na投人MgCl2溶液中出现的现象为(3)常温常压下制取100mL纯净的CO2,将其通入装有Na2O2粉末的硬质玻璃管中。①反应的化学方程式为②相同条件下,若反应后收集的气体体积为65mL,则反应消耗CO2的体积是mL.(4)现有一种以NaHCO3为主要成分的膨松剂,由于膨松剂存放时间较长,部分分解成Na2CO,粉末。为测定混合样品中NaHCO3的质量分数,按如图所示连接装置(装置的气密性良好,各装置中的试剂皆为足量)。K样品空气人收中处际西碱石灰AB浓硫酸碱石灰0E已知:碱石灰是固体氢氧化钠和氧化钙组成的混合物。实验过程:将m1g样品装入样品管中,测定实验前D的质量为m2g;打开K1、K2,关闭K,,缓缓鼓入空气数分钟,以除去装置中的二氧化碳;然后关闭K1、K2,打开K3,点燃酒精灯加热至不再产生气体;拆下装置,再次称量D的质量为m3g。①装置B中发生反应的化学方程式为②E处干燥管中盛放碱石灰的作用是如果没有该装置,可能会造成测定结果(填“偏高”“偏低”或“不变”)。③混合物中NaHCO3的质量分数为(用含m1、m2、m3的代数式表示)。【答案】(1)Na2CO3(1分)(2)有气体和白色沉淀产生(1分)【(3)①2Na2O2+2C02—2Na2C03+O2(1分)②70(2分)(4)①2NaHC0,△NaC0,+C0,↑+H,0(2分)9②防止空气中的CO2和水蒸气进入D中影响测定结果(2分)偏高(1分)③42m:-m2×100%(2分)4+11m1子中【解析】(1)空气中含有二氧化碳和水蒸气,在空气中的转化过程:Na→Na2O→NaOH→Na2CO3·10H2O→Na2 CO3,Na2O→NaOH→Na2CO3·10H2O→Na2CO3,Na2O2→NaOH+Na2C03·,10HzONa2CO3,NaOH→Na2CO3·l0H2O→Na2CO3,所以久置空气中最终都变为Na2CO3。(2)N与水反应生成氢氧化钠和氢气,氢氧化钠与氯化镁反应生成氢氧化镁沉淀和氯化钠。(3)①Na2O2与CO2反应生成碳酸钠和氧气,其反应的化学方程式为2Na2O2十2CO2一2Na2C03十O2。②根据反应:2C02+2Na2O2-2Na2C03+O2△V2VVx(100-65)mL解得x=70mL。(4)①装置B中为NaHCO,加热分解生成碳酸钠、二氧化碳和水,化学方程式为2 NaHCO,△Na,CO,十H2O+CO2↑。②干燥管中盛放的是碱石灰,碱石灰能吸收空气中的水蒸气和二氧化碳,所以干燥管的作用是防止空气中的CO2和水蒸气进入D中影响测定结果,如果没有这个装置将导致m?偏大,根据NaHCO3的质量分数计算式可知,导致结果偏高。③根据反应方程式可得4萨·置甲而麻置球面素答2NaHC0,△Na,C0,十H,0个+C02个家4,#长。家【2×8444(m3一m2)g造来长84×209M4442(m3-m2)42(m3-m2)建立关系式为,解得x=×100%。m3-m211,混合物中NaHCO3的质量分数为11m1

【答案】ABD【解析】k=8(20+12+13+15+16+14+12+18)=15,故A正确:0=。(25+9+4+0+1+1+9+9)=58√9,故B正确:4-30=15-3y2四2e+3=15+3则n-+]-5-3,15+293√292,20∈[μ-3a4+3a],12∈[4-3o,μ十3o],所以P1,P2都不是孤立点,故C错误,D正确.

以上就是英语周报高一3期答案2023,更多英语周报答案请关注本网站。
本文地址: http://www.ncneedu.cn/post/26423.html
文章来源:admin
版权声明:除非特别标注,否则均为本站原创文章,转载时请以链接形式注明文章出处。
- 04-05 1 英语周报八年级新目标答案第29期
- 04-05 2 英语周报八年级新目标scc答案5
- 04-05 3 英语周报答案七年级上册2022-2023
- 04-05 4 英语周报答案2022~2023
- 04-05 5 英语周报答案八年级下册2023
- 04-05 6 英语周报答案九年级人教版2023
- 02-24 7 时代英语报2022-2023 test7答案
- 02-24 8 双语报答案20222023高三
- 02-24 9 双语报浙江W版中考专版第35期答案
- 02-24 10 双语报英语答案高三课标24期
- 英语周报八年级新目标答案第29期
2023-04-05admin
- 英语周报八年级新目标scc答案5
2023-04-05admin
- 英语周报答案七年级上册2022-2023
2023-04-05admin
- 英语周报答案2022~2023
2023-04-05admin
- 英语周报答案八年级下册2023
2023-04-05admin
- 英语周报答案九年级人教版2023
2023-04-05admin
- 时代英语报2022-2023 test7答案
2023-02-24admin
- 双语报答案20222023高三
2023-02-24admin
- 双语报浙江W版中考专版第35期答案
2023-02-24admin
- 双语报英语答案高三课标24期
2023-02-24admin
