
初二八年级上册英语周报第22期答案


24.【考点】酸碱混合时的定性判断及有关pH的计算【分析】A.二者恰好完全反应时温度最高,则F点二者恰好完全反应,二者体积相等,且以1:1反应,所以二者浓度相等,则c=0.1B.F点溶液中溶质为NaX,Ⅹ2水解导致溶液呈碱性,水也电离生成OHC.G点溶液中溶质为等物质的量浓度的NaOH、Na2X,溶液中存在物枓守恒D.HX只电离不水解,则NaHX抑制水电离,Na2X促进水电离,NaOH抑制水电离【解答】解:A.二者恰好完全反应时温度最F点二者恰好完全反应,二者体积相等,且以1:1反应,所以二者浓度相等,则c=0.1,NaOH溶液的pH=13,故A正确B.F点溶液中溶质为Na2X,Ⅹ2-水解导致溶液呈碱性,水也电离生成OH,所以c(OH>c(HX-),故B正确C.G点溶液中溶质为等物质的量浓度的NaOH、Na2X,溶液中存在物料守恒,该二元酸第一步完全离,所以溶液中不存在HX,根据物料守恒得c(Na+)=3c(HXˉ)+3c〈Ⅹ2-),故C镨误D.HX只电离不水解,则NaH抑制水电离,Na2X促进水电离,NaOH抑制水电离,所以开始到F点水的电离程度增大、F到G点水的电离程度减小,故D正确故选:Ca点评】本题考査酸碱混合溶液定性判断,侧重考査图象分析判断及计算能力,明确水电离影响因素溶液中溶质成分及其性质是解本题关键,注意该二元酸第一步完全电离、第二步部分电离,为解答易错点
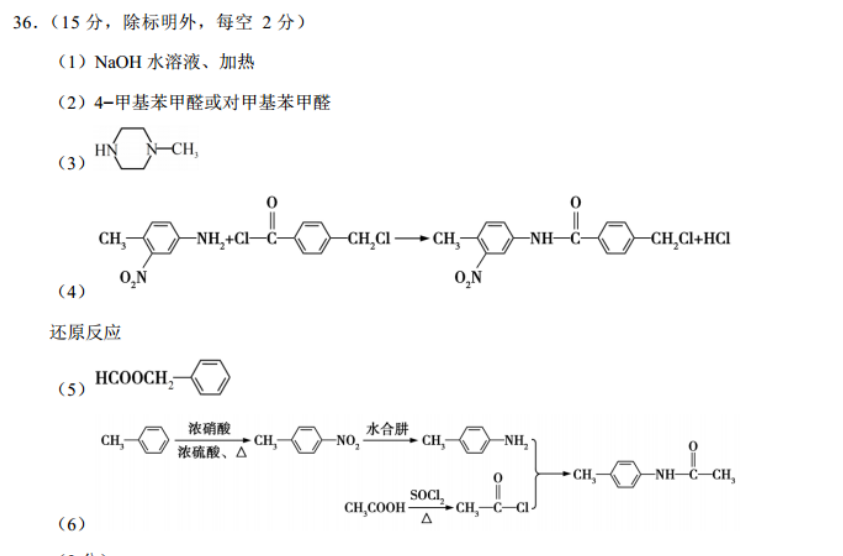
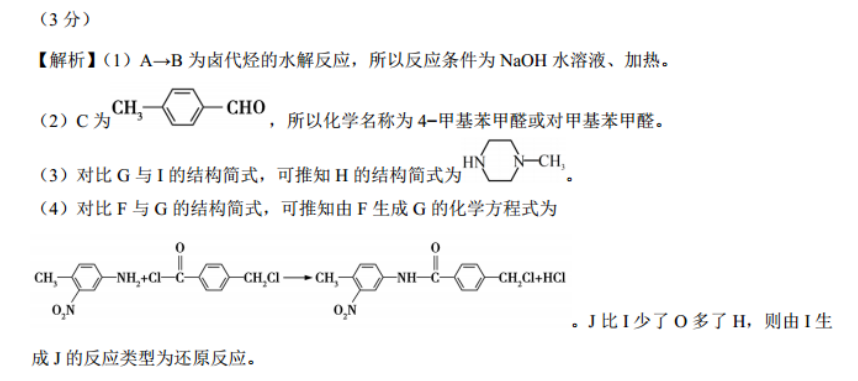
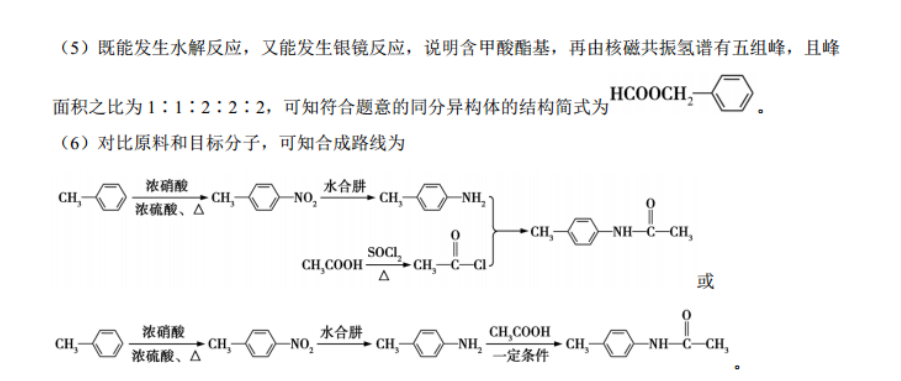
36.(15分,除标明外,每空2分)(1)NaOH水溶液、加热(2)4-甲基苯甲醛或对甲基苯甲醛-CH(3)00NH +CI-CCH Cl+HClON还原反应(5) HCOOCH浓硝酸水合肼浓硫酸、△CHCH》NH2NH-C-CHs00CH COOH-C-Cl(6)(3分)【解析】(1)A→B为卤代烃的水解反应,所以反应条件为NaOH水溶液、加热。(2)C为CHO,所以化学名称为4-甲基苯甲醛或对甲基苯甲醛HCH(3)对比G与I的结构简式,可推知H的结构简式为(4)对比F与G的结构简式,可推知由F生成G的化学方程式为0。J比I少了O多了H,则由I生成J的反应类型为还原反应。(5)既能发生水解反应,又能发生银镜反应,说明含甲酸酯基,再由核磁共振氢谱有五组峰,且峰面积之比为1:1:2:2:2,可知符合题意的同分异构体的结构简式为HCOOCH2(6)对比原料和目标分子,可知合成路线为浓硝酸浓硫酸、△①M水合肼CH- COOH或浓硝酸CH COOH浓硫酸、△①M水合时a①N一定条件

以上就是初二八年级上册英语周报第22期答案,更多英语周报答案请关注本网站。
本文地址: http://www.ncneedu.cn/post/18536.html
文章来源:admin
版权声明:除非特别标注,否则均为本站原创文章,转载时请以链接形式注明文章出处。
- 04-05 1 英语周报八年级新目标答案第29期
- 04-05 2 英语周报八年级新目标scc答案5
- 04-05 3 英语周报答案七年级上册2022-2023
- 04-05 4 英语周报答案2022~2023
- 04-05 5 英语周报答案八年级下册2023
- 04-05 6 英语周报答案九年级人教版2023
- 02-24 7 时代英语报2022-2023 test7答案
- 02-24 8 双语报答案20222023高三
- 02-24 9 双语报浙江W版中考专版第35期答案
- 02-24 10 双语报英语答案高三课标24期
- 英语周报八年级新目标答案第29期
2023-04-05admin
- 英语周报八年级新目标scc答案5
2023-04-05admin
- 英语周报答案七年级上册2022-2023
2023-04-05admin
- 英语周报答案2022~2023
2023-04-05admin
- 英语周报答案八年级下册2023
2023-04-05admin
- 英语周报答案九年级人教版2023
2023-04-05admin
- 时代英语报2022-2023 test7答案
2023-02-24admin
- 双语报答案20222023高三
2023-02-24admin
- 双语报浙江W版中考专版第35期答案
2023-02-24admin
- 双语报英语答案高三课标24期
2023-02-24admin
