
2018-2022学年英语周报八年级新目标第九期答案
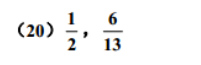
6(20)213




23.(13分)(1)MnO2+4H+2CI-Mn2*+CI 1+2H,O(2分)(2)ahifgbcedlmj(k)(2分)(3)饱和食盐水(1分)③①②(2分)(4)牛角管(1分)吸收多余的氯气,并防止空气中的水蒸气进入装置G(1分)(5)3SnCl4+2H2O=SnO2(胶体)+2H2[SnCl6(2分)(6)①甲基橙(1分)26.16mol·L1(1分)【解析】(1)装置A中发生反应的离子方程式为MnO, +4H++2Cr4-Mn2++C1++2H20(2)装置A制取Cl2,制得的Cl2中混有HCl和H2O(g),装置E(盛有饱和食盐水)除去HCl,装置D除去H2O(g),装置B制取无水四氯化锡,制得的无水四氯化锡呈液态,混有未反应完的液态锡,将其进行蒸馏,在装置G中得到纯净的无水四氯化锡,蒸馏过程中需要用到装置C中的冷凝管,装置G后连接装置F,用于吸收多余的氯气,并防止空气中的水蒸气进入装置G。故装置的连接顺序为 ahifgbcedlmj(k)。(3)装置E中盛装的试剂为饱和食盐水;反应开始前应先打开恒压滴液漏斗活塞,加热装置A处的酒精灯,用生成的氯气将装置中的空气排出,再点燃装置B处的酒精灯。(4)装置G中仪器X为牛角管。装置F的作用为吸收多余的氯气,并防止空气中的水蒸气进入装置G。(5)向四氯化锡中慢慢加水生成SnO2胶体和六氯合锡酸(H2[SnCl6]),该反应的化学方程式为3SnCl4+2H2O=SnO2(胶体)+2H2[SnCl4]。(6)①Mn2开始沉淀的pH为5.2,小于7.0,故需要选择在酸性条件下变色的指示剂,最好选用甲基橙作指示剂。②滴定终点消耗0.2000mo·L-1NaOH溶液的体积为19.25mL,根据关系式:NaOH~HCl可知,反应后溶液中剩余HCl的物质的量为0.2mol·L1×0.01925Lx400ml0.0616mol,浓度为Q.0616mol0.01L6.16mol·L-1。

以上就是2018-2022学年英语周报八年级新目标第九期答案,更多英语周报答案请关注本网站。
本文地址: http://www.ncneedu.cn/post/22567.html
文章来源:admin
版权声明:除非特别标注,否则均为本站原创文章,转载时请以链接形式注明文章出处。
- 04-05 1 英语周报八年级新目标答案第29期
- 04-05 2 英语周报八年级新目标scc答案5
- 04-05 3 英语周报答案七年级上册2022-2023
- 04-05 4 英语周报答案2022~2023
- 04-05 5 英语周报答案八年级下册2023
- 04-05 6 英语周报答案九年级人教版2023
- 02-24 7 时代英语报2022-2023 test7答案
- 02-24 8 双语报答案20222023高三
- 02-24 9 双语报浙江W版中考专版第35期答案
- 02-24 10 双语报英语答案高三课标24期
- 英语周报八年级新目标答案第29期
2023-04-05admin
- 英语周报八年级新目标scc答案5
2023-04-05admin
- 英语周报答案七年级上册2022-2023
2023-04-05admin
- 英语周报答案2022~2023
2023-04-05admin
- 英语周报答案八年级下册2023
2023-04-05admin
- 英语周报答案九年级人教版2023
2023-04-05admin
- 时代英语报2022-2023 test7答案
2023-02-24admin
- 双语报答案20222023高三
2023-02-24admin
- 双语报浙江W版中考专版第35期答案
2023-02-24admin
- 双语报英语答案高三课标24期
2023-02-24admin
